HeLa细胞的前世今生,你知道吗?
提起HeLa细胞,学生物的你一定不陌生。这是一种宫颈癌细胞的细胞系,被广泛应用于肿瘤研究、生物实验或者细胞培养。但是,HeLa细胞又有着许多的传奇故事,你知不知道呢?
起源之时
1951年,美国马里兰州的一位妇女海瑞塔·拉克丝(Henrietta Lacks)因为腹痛,到附近的约翰·霍普金斯医院进行检查。医生在她的子宫颈上发现了一个紫色的肿瘤。这个“紫葡萄”模样的肿瘤表面光滑,稍微一碰就会流血。经诊断,拉克丝属于晚期宫颈癌,并很快做了手术。
但拉克丝并不知道,当她躺在手术台上的时候,实施手术的外科医生还做了另一件事情。在没有告知患者的情况下,这位医生取下了肿瘤组织的样本。当时,他正因为对良性肿瘤的激进治疗而备受争议,他希望对不同类型的宫颈癌细胞进行培养,从而证明自己的论断。
样本被送到医院的组织培养研究中心。研究中心的乔治·盖伊(George Gey)正在进行另外一项研究:在人体外培养癌症细胞,以解释癌症产生的原因,从而找到治疗方法。在过去的30年里,盖伊和同事们尝试培养了许多癌细胞,但每次那些癌细胞总是很快死掉,即使有少量的“幸存者”,它们也根本不会生长,无法满足研究的需要。
可拉克丝的癌细胞却出现了例外:在培养的第二天,它们就出现了生长的迹象。随后研究员们兴奋地发现,这些癌细胞似乎有着无限生长的能力:每隔24小时数量就增加一倍。盖伊知道,这就是他要找的“长生不老”细胞。盖伊博士分别取海瑞塔·拉克丝的姓和名的前两个字给细胞命名。从此,海瑞塔·拉克丝变成了海拉(HeLa)。在不到两年的时间里,HeLa细胞迅速传遍世界,成为无数科学家的研究工具。
传奇之路
HeLa细胞系被George Gey分送给众研究单位,并用作癌症模式细胞研究。HeLa细胞系也被用作研究细胞信号传导,在几十年的研究过程中,HeLa细胞帮助科学家们开创了许多传奇的故事。
改变遗传学
1953年,一位用HeLa细胞进行实验的研究人员发现,一种名为苏木素的着色剂能够让细胞核的染色体清晰可见,这是科学家首次发现原来人体是有46条染色体的。利用这一发现,科学家成功找出了唐氏综合症等疾病的遗传联系,并逐渐掌握遗传性疾病的诊断方法。
实现细胞克隆
1954年,HeLa细胞帮助科学家实现了细胞克隆。当我们听到“克隆”一词,首先想到的是克隆羊多利。其实在克隆动物之前,最早被克隆的是HeLa细胞。科学家利用其具有顽强生命力的特征,发明了一种分离单一细胞的方法,并让其存活足够长的时间来复制和创造一个自身的完美拷贝。这一重大突破为动物克隆、基因疗法、试管受精和干细胞分离等生物医学技术奠定基础。
飞向太空
1956年,HeLa细胞先于人类,随一颗前苏联卫星进入太空,开始被用于太空生物学研究。美国宇航局后来还在首次载入航天飞机中携带了HeLa细胞,并发现癌细胞在太空中繁殖更快。
实现基因混合
1965年,科学家通过将HeLa细胞和小鼠细胞融合,人类首次创造了跨物种混合体。基因混合技术不仅让人们可以开始绘制人类基因图谱、进行血型鉴定,也带动了抗癌药物赫塞汀的发明。基因混合技术的实现催生了全球科学家参与的人类基因组计划。

奠定HPV疫苗的诞生
1984年,德国病毒学家哈拉尔德·楚尔·豪森发现人类乳头瘤病毒新种HPV-18,他认为是HPV-18和HPV-16引发了子宫颈癌。豪森检测了拉克丝的活组织切片,发现拉克丝感染了HPV-18病毒。科学家们随后又利用HeLa细胞研究了HPV病毒的致病机理,他们发现HPV会将自己的DNA插入宿主细胞的DNA中,然后表达蛋白导致癌症产生。他们还发现当HPV的DNA被抑制时,宫颈癌细胞停止癌变。这些发现促使了HPV疫苗的产生,也为哈拉尔德·楚尔·豪森赢得了诺贝尔奖。

永生之谜
HPV的研究也最终揭开了拉克丝得癌症的原因:HPV病毒DNA插入了她的11号染色体,导致p53基因的关闭,引发癌症。p53是一种肿瘤抑制基因,它编码的蛋白能够抑制突变和肿瘤的发生。一旦发生突变,p53便失去了对细胞生长、凋亡和DNA修复的调控作用,导致细胞癌变。在所有恶性肿瘤中,50%以上会出现该基因的突变。
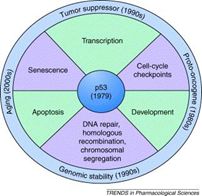
HPV病毒在肿瘤发生中起重要作用,几乎所有的宫颈癌都是有它引起的。HPV的基因表达产物能够间接激活端粒酶,而HeLa细胞的永生之迷就在“端粒酶”。

端粒酶在细胞中负责端粒的延长。端粒是染色体末端的一种特殊结构,在正常人体细胞中,端粒随着细胞分裂而逐渐缩短,其长短和稳定性决定了细胞寿命,与细胞衰老和癌变密切相关。Hela细胞经历细胞分裂时可维持端粒酶活性,端粒酶不断地延长HeLa细胞染色体的端粒,使其快速分裂,并可以无限增殖下去。
伦理之争
目前,人们已经很难计算,世界上到底存在着多少个HeLa细胞。美国一家专门出售HeLa细胞的公司,每周产量有两万盒,里面有超过6万亿个细胞。还有科学家估计说,如果我们能把所有的HeLa细胞都集合起来,它们的重量会超过5000万吨——这相当于100个帝国大厦的重量。
相比之下,细胞的主人拉克丝却一直默默无闻。直到2010年2月,一本记录这个传奇故事的书籍《永生的海拉》在美国出版,这位细胞之母才真正进入公众视野。但海瑞塔·拉克丝这名贫穷、教育程度低的黑人,生前从未对自己细胞用于研究表示过同意。几十年来,她的家属一直被排除在有关研究的决策过程之外。直到 1973 年科学家们打来电话,请求提取血液样本用于研究她的孩子从她那里遗传获得的基因的时候,拉克斯女士的家属才获悉,他们母亲的细胞实际上已经遍布全球。
而今,美国国家卫生研究院在已与拉克斯家族达成协议,将拉克斯基因组使用的决定权授予他们。这一协议是拉克丝传奇中的一个里程碑。它也让人们注意到,在基因研究的益处和基因被研究的人士(及其亲属)隐私权受侵犯的风险之间,尚欠缺一些保持平衡的政策。
污染之王
除了为生命科学领域的研究带来极大便利,HeLa细胞也因其特性干扰和毁掉了许多的研究成果。1966年Stanley Gartler通过对同工酶表达水平的鉴定,首次提出来源于18个独立个体的细胞系,如正常肠上皮细胞(Int-407)、正常羊膜细胞(WISH)、正常肝细胞(Chang liver)、喉癌(Hep-2)和口腔癌(KB),可能全是Hela细胞的观点。1981年,科学家Walter Nelson-Rees在利用核型分析对细胞进行鉴定后,才证实了细胞库中的一系列细胞系确实存在着大量的HeLa细胞交叉污染,并将该成果发表于Science期刊上。Walter Nelson-Rees毕生都在研究控制HeLa细胞蔓延的方法,但临终前承认自己的努力是徒劳的,并称HeLa细胞“像是在某个地方跳舞”,永不灭亡。
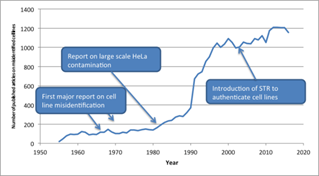
HeLa细胞蔓延的问题现在也没有得到解决。所以,HeLa细胞就因经常更换马甲且混迹在各类细胞系中,而被冠以了细胞界“隔壁老王”的称号。好了,HeLa细胞前世今生的故事就讲到这里。对比细胞房里的其他细胞,你一定在感谢自己的HeLa细胞是这么好养活。但是也请别忘记,这株细胞背后还有这么多的传奇故事。除了HeLa细胞,还有许多其他细胞系在不同“外衣的伪装”下盛行于世界各地的实验室。许多研究领域(尤其是肿瘤学、生物化学/分子生物学,药理学和细胞生物学等领域)的研究者都深受其害。
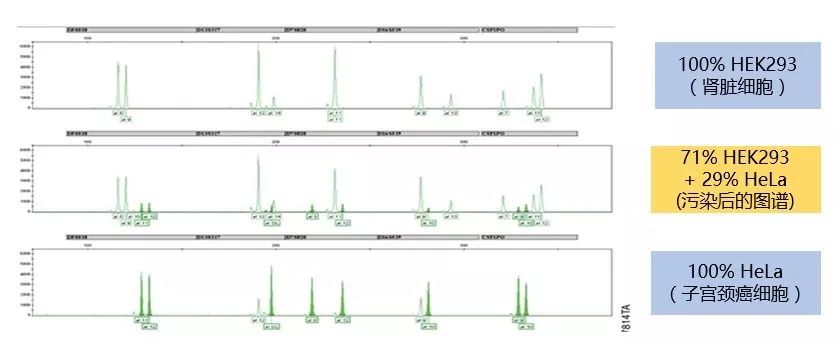
目前,ICLAC、ATCC等权威机构鉴定细胞系的“金标准”是通过STR(Short Tandem Repeat,短串联重复序列)分型来做细胞鉴定。拥有多年基因组学服务经验的金唯智,可以为您提供全面专业的细胞系鉴定服务:
- 人源细胞系来源一致性检测(两种细胞样品);
- 人源细胞STR分型检测/ ATCC细胞系鉴定(9基因座,10基因座,16基因座);
- 人鼠细胞交叉污染检测(人源细胞中是否有小鼠源细胞污染;干细胞中是否存在小鼠源饲养层细胞)。
金唯智现已为国内外多所高校、科研院所以及生物医药企业提供过细胞系鉴定服务,并已有多篇文章发表。